Клінічні дослідження (інша назва «клінічні випробування») обов’язково проводяться за участі людей. Вони спрямовані на оцінку медичного – фармакологічного, хірургічного, або поведінкового втручання. Такі дослідження є основним способом, за допомогою якого вчені з’ясовують, чи є новий засіб лікування, наприклад, новий лікарський препарат, дієта чи медичний пристрій (наприклад, кардіостимулятор нової моделі) достатньо безпечним та ефективним для людей. Часто клінічне дослідження використовують для того, щоб дізнатись, чи нове лікування є більш ефективним а також чи має воно менш шкідливі побічні ефекти, ніж стандартне лікування.
У ході інших клінічних досліджень вчені перевіряють способи раннього виявлення захворювання, іноді ще до появи симптомів. Клінічні дослідження ще одного типу перевіряють способи запобігання проблемам зі здоров'ям. Клінічне дослідження може також розглянути питання, як покращити життя людей, які живуть із захворюваннями, що загрожують життю, або хронічними проблемами зі здоров'ям. Зазвичай у клінічному дослідженні можуть брати участь хворі люди (пацієнти), здорові люди або і ті, й інші.
Перш ніж регуляторний орган тієї чи іншої країни (наприклад відповідний комітет у складі міністерства охорони здоров’я) затвердить початок клінічного випробування, вчені проводять лабораторні дослідження та дослідження на тваринах, щоб перевірити потенційну безпеку та ефективність терапії. Якщо ці дослідження показують сприятливі результати, регуляторне відомство країни дає згоду на тестування, яке має бути перевірене на людях.
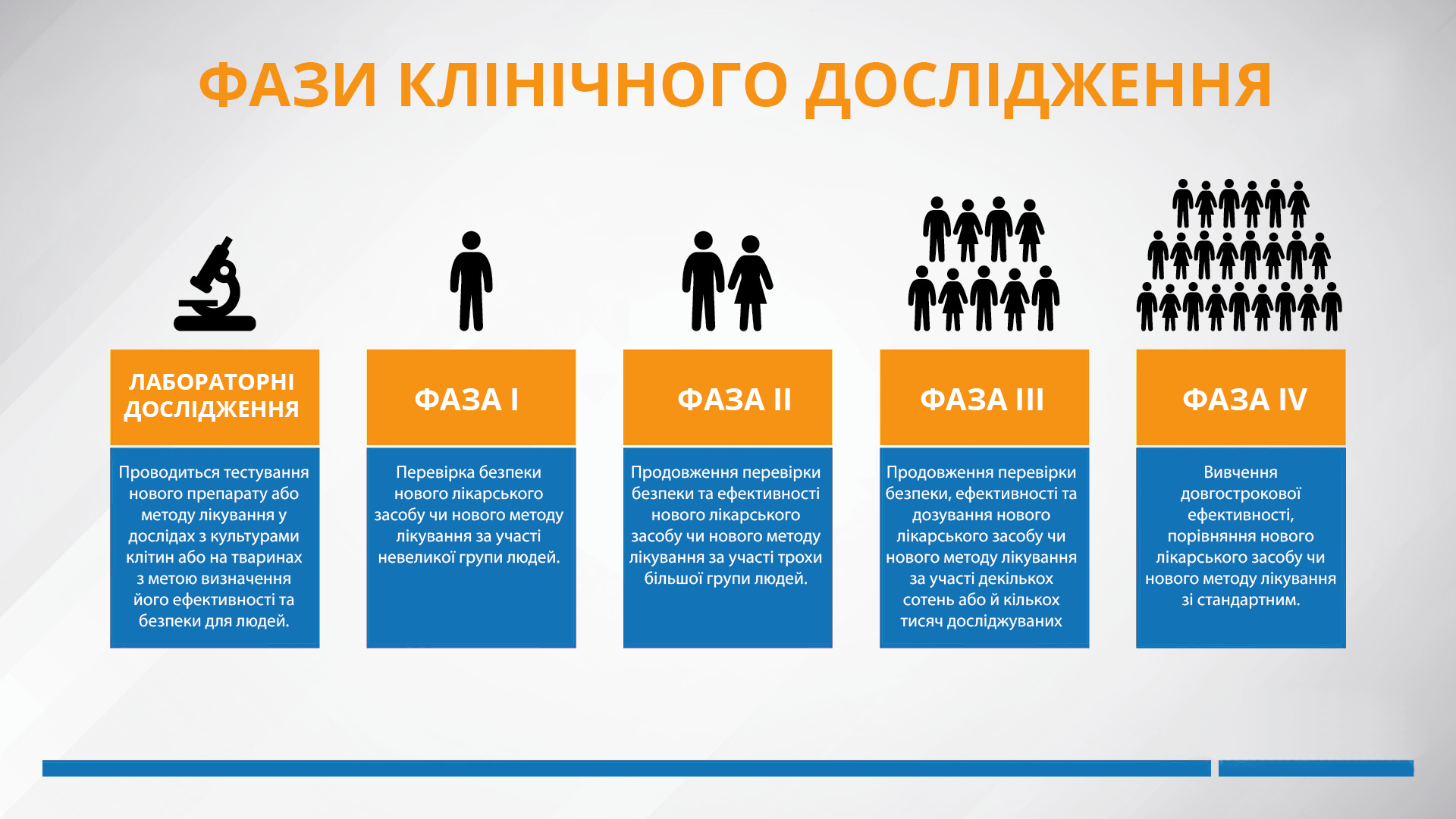
Клінічні дослідження – процес довгочасний; зазвичай на випробування нового препарату потрібно щонайменше декілька років. Згідно з практикою, яка використовується у всьому світі, клінічні дослідження проходять чотири етапи або 4 фази – в залежності від їх мети і кількості учасників (Рис. 1).
I фаза клінічних досліджень майже не проводиться в Україні. Це дослідження, у якому безпека препарату і тривалість зберігання препарату в організмі тестується на незначній групі добровольців
II фаза досліджень також в Україні проводиться рідко. У таких дослідженнях безпека, ефективність і дозування препарату досліджується на невеликій групі пацієнтів із певним захворюванням.
III фаза клінічних досліджень найчастіше проводиться в Україні. У цих дослідженнях бере участь велика кількість пацієнтів із певним захворюванням. Проводиться підтвердження ефективності та дозування препарату, а також виявлення побічних ефектів.
IV фаза досліджень проводиться після реєстрації препарату. Визначається характер його взаємодії з іншими препаратами, продуктами харчування для широкого застосування та безпеки.
Є багато причин, чому люди вирішують стати учасниками клінічного випробування. Деякі приєднуються до клінічного дослідження через те, що стандартне лікування їхнього захворювання, не дало результату. Інші беруть участь, оскільки не існує методів лікування їхньої хвороби (наприклад, у випадку рідкісних захворювань). Беручи участь у клінічному випробуванні, учасники можуть дізнатись про нові методи лікування, перш ніж вони стануть широко доступними. Деякі дослідження призначені для людей, які здорові, але хочуть допомогти знайти способи запобігання захворюванню, наприклад, такому, яке може бути поширеним у їхній родині.
Якою б не була мотивація, коли людина вирішує взяти участь у клінічному випробуванні, вона стає партнером у науковому відкритті. І її внесок може допомогти прийдешнім поколінням вести здоровіший спосіб життя. Великі медичні прориви не могли б відбутися без великодушності, безкорисливості і навіть певної самопожертви учасників клінічних випробувань – молодих та старих.
В Україні порядок проведення клінічних випробувань лікарських засобів та експертизи матеріалів клінічних випробувань встановлений відповідним наказом міністра охорони здоров’я України. Перш, ніж набути чинності, такий наказ повинен пройти в установленому порядку державну реєстрацію в Міністерстві юстиції України.
Основний принцип, яким повинні керуватись організатори клінічних досліджень в Україні чи будь-якій іншій країні, відомий в медицині з давніх давен: «Primum non nocere!», тобто «Насамперед не спричини пацієнту (у цьому випадку учаснику клінічного дослідження) шкоди!»
Інакше кажучи, в Україні всі клінічні випробування проводяться відповідно до міжнародних етичних принципів із забезпеченням захисту прав, безпеки та благополуччя досліджуваних. Клінічне випробування може проводитись тільки в тому випадку, якщо очікувана користь виправдовує ризик.
Згідно наказу міністра охорони здоров’я України, процедура захисту інтересів учасників дослідження є детально визначеною і передбачає надання інформації пацієнтам (здоровим добровольцям) про клінічне випробування та одержання від них інформованої згоди у письмовому вигляді. Крім того, пацієнт (здоровий доброволець) або законний представник/близький родич повинен одержати вичерпні відповіді на всі питання щодо клінічного дослідження.
У ході самого дослідження всі дані про учасника зберігаються в таємниці та обробляються в межах клінічного випробування у знеособленому вигляді, що забезпечує право досліджуваних на конфіденційність інформації про стан їхнього здоров’я.
Наказ міністра охорони здоров’я про порядок проведення клінічних досліджень окрім суто технічних моментів приділяє велику увагу дотриманню виконання етичних норм у ході таких досліджень у кожному лікувальному (або лікувально-профілактичному) закладі, де вони проводяться. Оцінка етичних та морально-правових аспектів клінічного дослідження здійснюється спеціальними комісіями з питань етики при таких лікувальних закладах.
Звичайно, що не менша увага приділяється у цьому документі і безпеці учасників дослідження. Так, наприклад, під час проведення клінічного випробування відповідальний дослідник зобов’язаний терміново повідомляти розробника нового препарату про всі серйозні побічні явища, крім тих, які у протоколі або брошурі дослідника визначені як такі, що не потребують негайного повідомлення.
Клінічні дослідження допомагають лікарям зрозуміти, як краще лікувати ту чи іншу хворобу. Це може принести користь як самим учасникам таких досліджень, так і іншим людям з таким самим діагнозом.
Якщо пацієнт берете участь у клінічному дослідженні, він може бути одним із перших, хто отримає реальну користь від нового методу лікування чи нового препарату.
Клінічні випробування забезпечують найкоротший шлях для нових лікарських засобів, які часто стають єдиним порятунком для тяжкохворих людей, від дослідницької лабораторії до широкого впровадження в клінічну практику.