Хартмут Векерле,
Институт микробиологии имени Макса Планка, г. Мартинсрид, ФРГ
Реферат
В-лимфоциты играют исключительно важную роль в патогенезе рассеянного склероза (РС). Они регулируют аутоиммунную реакцию и участвуют в развитии очагов поражения (демиелинизации) в центральной нервной системе. В данном обзоре рассматриваются особенности В-клеток и их функции в развитии РС, а также содержится описание процесса накопления аутоиммунных В-клеток в веществе головного мозга.
Согласно существовавшим ранее представлениям, РС является аутоиммунным демиелинизирующим заболеванием, при котором реактивные к собственному миелину Т-клетки проникают в ЦНС извне и провоцируют изменения воспалительного характера, приводящие в конечном итоге к образованию очагов демиелинизации. Большинство стратегий лечения РС были направлены на уничтожение таких патогенных Т-клеток или на подавление их активности. Меньше внимания уделялось той роли, которая в аутоиммунном патогенезе принадлежит аутоиммунным В-клеткам.
Сегодня ключевые роли аутоиммунных В-клеток в патогенезе РС подтверждены мощной доказательной базой, краткое изложение которой приведено в первой части данного обзора. Во второй части содержится описание экспериментальных исследований аутоиммунных процессов в головном мозге. Такие исследования проводились на модели трансгенных мышей. Подобные процессы относятся к экспериментальному аутоиммунному энцефаломиелиту (ЭАЭ), который может быть связан с возможным участием аутоиммунных В-клеток и их рекрутингом из общего иммунного репертуара В-клеток.
В-клетки в очагах демиелинизации при РС
В-клетки являются обычным компонентом иммунных инфильтратов, обнаруживаемых в активных очагах поражения на ранних стадиях развития РС. Они представляют собой относительно немногочисленную субпопуляцию, обнаруживаемую в головном и спинном мозге, которая главным образом входит в состав скоплений клеток вокруг кровеносного сосуда. Кроме того, такие В-клетки диссеминируют в окружающую паренхиму. Они также образуют плотные конгломераты в субарахноидальной полости, покрывающие поверхность коры. Некоторые из таких конгломератов могут иметь организованную структуру, напоминающую строение зародышевых центров.
Скопления В-клеток в субарахноидальной полости являются характерным признаком прогрессирующего РС, хотя такие скопления обнаруживаются и на ранних стадиях рецидивирующе-ремиттирующей формы этого заболевания. Многообразие патогенных функций аутоиммунных В-клеток представлены во врезке 1.
Олигоклональные группы в спинномозговой жидкости
Ткани ЦНС постоянно омываются межклеточной (тканевой) жидкостью, которая проникает в спинномозговую жидкость (СМЖ). В норме СМЖ обеспечивает транспорт структур ЦНС и метаболитов, однако в ней отсутствуют иммуноглобулины и другие белки плазмы. Вместе с тем, важно отметить, что при РС СМЖ обычно содержит иммуноглобулины в виде отдельных полос, а не в виде сплошной массы как в плазме. Поскольку при РС появление олигоклональных полос является неизбежным, они представляют ценность как биомаркер этого заболевания. Однако до сего времени не были идентифицированы ни их антигены-мишени, ни их клеточное происхождение.
Dornmair с соавторами использовали сочетание метода транскриптомики, который позволил определить характеристики генного репертуара иммуноглобулинов у индивидуальных В-клеток СМЖ, с методом протеомического секвенирования изолированных полос олигоклональных иммуноглобулинов. В результате эти исследователи смогли доказать, что большинство олигоклональных полос происходят от местных В-клеток, а также В-клеток, обитающих в СМЖ либо в паренхиме.
Нескольким группам ученых удалось клонировать парные гены иммуноглобулинов СМЖ и получить рекомбинантные антитела. Скрининг на антигены-мишени дал неоднозначные результаты. Одна группа определила как связующее звено широко распространенные внутриклеточные белки, в то время как другие исследователи пришли к выводу, что детерминантой связывания являются липиды. Вместе с тем, поиск антител, реагирующих на основные миелиновые структуры, закончился неудачей во всех исследованиях.
ЦНС – «убежище» для В-клеток?
Олигоклональные группы (зоны олигоклональных иммуноглобулинов) формируют очень характерные образования у каждого пациента с РС; достаточно необычно то, что такие образования остаются неизменными на протяжении многих лет. Такая стабильность не может не вызывать удивления, поскольку принято считать, что паренхима ЦНС является микросредой, которая не способна поддерживать длительное выживание иммунных клеток. Однако, живучесть олигоклональных групп дает основания полагать, что В-клетки, секретирующие иммуноглобулины, как и их клоны, могут выживать в этой ткани в течение продолжительного времени. Это дает основания полагать, что микросреда ЦНС является биотопом, вполне благоприятным для В-клеток.
Meinl с соавторами более чем успешно доказали, что астроциты, основные многофункциональные клетки глии, способны вырабатывать факторы роста В-клеток, включая BAFF, CXCL10 и CXCL13 (это может способствовать выживанию В-клеток) и что воспалительный процесс усиливает их выработку. Вместе с тем, резидентные В-клетки ЦНС не образуют полностью изолированную популяцию, и, по всей видимости, между ними и периферийными популяциями В-клеток происходит взаимный обмен. Это было подтверждено недавним исследованием, в ходе которого было проведено глубокое секвенирование, позволившее идентифицировать гены сходного происхождения в ЦНС и в периферийных клетках.
Врезка 1. функции В-клеток при аутоиммунной болезни.
Секреция патогенных аутоантител
Механизмы:
- комплементзависимое уничтожение клеток-мишеней;
- блокада поверхностных структур (прямая в слепом режиме или с помощью интернализации рецепторов);
- связывание комплекса аутоантигена с антиген-представляющими клетками.
Доказательства:
- нейромиелит зрительного нерва (антитела к аквапорину 4);
- аутоиммунный энцефалит: антитела к антинейрональному рецептору (N-метил-D-аспартат [NMDA], альфа-амино-3-гидрокси-5-метил-4-изоксазол-пропионовая кислота [AMPA], гамма аминобутировая кислота (GABA) и т.д.
- РС: (патогенных аутоантител на данный момент не выявлено).
Презентация антигенов
- Механизмы: (растворимые антигены, связанные с иммуноглобулинами на поверхности В-клетки [специфические антитела], концентрированные и подготовленные для презентации аутоиммунным Т-клеткам);
- Доказательства: мышиная модель спонтанного развития экспериментального аутоиммунного энцефаломиелита (ЭАЭ); презентация антигена in vitro;
- РС: CD40/IL-4 активированная B-APC представляет антиген Т-клеткам типа CD4+ (преференции не обнаружены);
Выброс цитокинов
- Механизмы: выделяемые В-клетками цитокины/хемокины воздействуют на локальную иммунную микросреду;
- регуляторные В-клетки: выделяют противовоспалительнные цитокины (IL-10, TGF-b);
- противовоспалительные В-клетки: выделяют такие цитокины как GM-CSF, которые поддерживают воспалительные (ауто)иммунные реакции;
Доказательства: изоляция из организма мышей, перенесших нежелательное внешнее явление, перенос защиты;
РС: изоляция популяций клеток памяти CD4+ из лимфоцитов периферической крови.
Транспорт аутоантигена:
Механизм: антиген-специфические В-клетки захватывают антигены с помощью рецепторов на поверхности антигена и переносят их в фолликулы селезенки и/или лимфатических узлов;
Доказательства: экспериментальные системы;
РС: данных нет.
Антигены – «мишень» для В-клеток
Имеются косвенные доказательства того, что, по крайней мере у части пациентов, терапия гуморальными антителами приводит к поражению тканей из-за их связывания с клетками головного мозга и последующего разрушения таких клеток в зависимости от действия компонентов (факторов) комплемента.
Во-первых, Lucchinetti с соавторами обнаружили присутствие активированного комплемента C’9neo на структурах поврежденной ткани бляшек РС основного класса, что указывало на реакцию антитело/антиген. Во-вторых, в ходе исследования с ограниченной когортой пациентов с реакцией-ответом подобного типа, подтвержденной с помощью биопсии, было установлено, что плазмаферез уменьшает неврологический дефицит. В-третьих, в кортикальных зонах, расположенных под субарахноидальными агрегатами В-клеток, наблюдались процессы демиелинизации и дегенерации нейронов, что, по всей вероятности, было вызвано диффузией гуморальных факторов (антител) в ткань. И, наконец, анти-C20 антитела, вызывающие уменьшение популяции В-клеток (ритуксимаб), стали мощным лекарственным средством для терапии РС на ранней стадии, которое значительно снижает частоту рецидивов, уменьшает степень демиелинизации, определяемую радиологически, и улучшает неврологический дефицит.
Целевые антигены при РС с участием В-клеток на протяжении долгого времени являлись предметом научных споров. В то время как в ходе исследований, посвященных свойствам рекомбинантных антител, была обнаружена способность олигоклональных иммуноглобулинов СМЖ вступать в реакцию с некоторыми внеклеточными структурами, авторы этих исследований не обнаружили связывания с каким-либо известным миелином или другими антигенами глии. Это поставило под большое сомнение способность рекомбинантных антител выступать в роли классических демиелинизирующих антител.
С другой стороны, существуют научные публикации, указывающие на возможную роль в этом процессе антител ионных каналов и синаптических структур. В ходе тщательно проведенного исследования Hemmer с соавторами обнаруживали у значительного количества пациентов с ремиттирующим-рецидивирующим РС аутоантитела против глиального калиевого канала KIR4.1, хотя в других когортах подобное явление отсутствовало. Затем было также установлено, что у части больных происходила выработка антител против антигенных детерминант, расположенных вокруг аксональных узелков. Наиболее загадочной мишенью является миелиновый олигодендроцитарный гликопротеин (МОГ) основной энцефалитоген в случае мышиной модели экспериментального аутоиммунного энцефаломиелита (ЭАЭ), который из-за его расположения на поверхности миелина является полностью доступным для гуморальных антител. Появление аутоантител против МОГ является отличительным признаком РС детского возраста и острого диссеминированного энцефаломиелита (ОДЭМ). Аутоантитела против МОГ были также обнаружены у больных с аквапорин-4 отрицательным нейромиелитом зрительного нерва, а в последнее время также и при недавно открытых демиелинизирующих заболеваниях, обладающих признаками и РС, и аквапорин-4 отрицательного нейромиелита зрительного нерва. Примечательно, что человеческие антитела против МОГ являются видоспецифическими – они распознают конформационные эпитопы на МОГ человека, но не реагируют на МОГ грызунов.
Экспериментальные модели аутоиммунных нарушений головного мозга
Возникают имеющие большое значение вопросы о механизмах, которые приводя к рекрутингу аутоиммунных В-клеток при спонтанном развитии аутоиммунных заболеваний головного мозга, и о роли этих клеток в патогенезе таких заболеваний. Участие В-клеток в развитии аутоиммунных нарушений может проявляться секрецией поврежденных аутоантител, а также переносом аутоантигена из тканей во вторичные органы иммунной системы, презентацией антигена Т-клеткам и выделением цитокинов, воздействующих на ткани в очаге демиелинизации.
Возможно, для ответа на эти вопросы клинических исследований будет недостаточно, кроме того классические модели ЭАЭ в данном случае имеют ограниченную ценность, принимая во внимание искусственный характер индукции иммунного ответа (адъювантная иммунизация, перенос иммунных клеток). В качестве альтернативы мы разработали 2 модели исследования с использованием трансгенных мышей, обладающих склонностью к спонтанному развитию ЭАЭ. В таких моделях используется взаимодействие Т-клеток и В-клеток.
Мыши OSE являются мышами линии C57BL/6 с двойной трансгенностью, у которых имеются Т-клетки, реагирующие в отношении МОГ, обладающие МОГ-специфичным рецептором, а также встроенной в их В-клетки МОГ-специфичной цепью Н. У таких мышей заболеваемость ЭАЭ приближается к 60%, причем очаги демиелинизации локализованы в зрительном нерве и спинном мозге и практически не затрагивают головной мозг.
В отличие от мышей OSE мыши RR относятся к линии SJL/J с одной трансгенностью, у которых t-клеточные рецепторы реагируют на МОГ. У мышей RR такие рецепторы экспрессируются на > 70% клеток CD4 T. Почти у 100% мышей RR происходит спонтанное развитие ремиттирующего-рецидивирующего РС. И у мышей OSE, и у грызунов RR развитие заболевания в значительной мере зависит от наличия интактной кишечной микрофлоры. При полном отсутствии микробиоты кишечника развития ЭАЭ не происходит, однако после колонизации с помощью «чужого» помета болезнь развивается очень быстро.
В-клетки играют значительную роль в этих обеих животных моделях ЭАЭ. У мышей OSE В-клетки захватывают водорастворимый антиген даже если он присутствует в очень разбавленном виде, концентрируют его и представляют его распознанным Т-клеткам, что в результате приводит к усилению процесса аутоиммунного ответа. В противоположность этому у мышей RR роль В-клеток сводится к выработке демиелинизирующих антител.
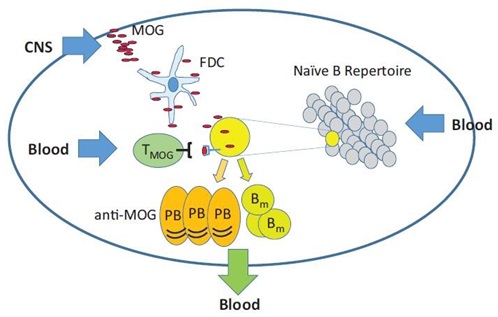
Рисунок 1. Рекрутинг аутоиммунных клеток, направленных против миелин-олигодендроцитарного гликопротеина (МОГ), в процессе дренажа из ЦНС в шейные лимфатические узлы (ЛУ). Рекрутинг В-клеток зависит от прохождения активированных МОГ специфических Т-хелперов по кровеносным либо по лимфатическим сосудам, так же, как и от материала, содержащего МОГ, транспортируемого из мозга по лимфатическим сосудам (материала растворимого, в форме частиц, либо перемещаемого фагоцитами).
Такие мыши RR обладают удивительными свойствами, поскольку они появляются на свет с оригинальным нетрансгенным иммунным репертуаром В-клеток, однако когда животные достигают возраста приблизительно 4-х недель, в плазме их крови появляются анти-МОГ аутоантитела. Такие антитела способны распознавать конформационные эпитопы МОГ на поверхности миелина, а после их трансплантации мышам-реципиентам с незначительными очагами поражения без демиелинизации вызывают появление больших сливающихся бляшек с выраженным разрушением миелина, которые очень напоминают бляшки, образующиеся у людей с РС.
В-клетки играют огромную роль в таком патогенезе, о чем свидетельствует тот факт, что у мышей RR, лишенных популяции В-клеток, не происходит развития рецидивирующего ЭАЭ. Рекрутинг МОГ-реактивных В-клеток зависит от наличия МОГ: у мышей с полной экспрессией Т-клеточного рецептора, у которых отсутствует МОГ, антитела против МОГ не образуются. Вторичное образование антител зависит от микробиоты: у безмикробных мышей не образуются аутоантитела против МОГ и не развивается ЭАЭ.
Обе эти животные модели ЭАЭ предоставляют ученым уникальные возможности для изучения процесса рекрутинга, распространения и активизации аутоиммунных В-клеток (Рисунок 1). В частности, благодаря спонтанности развития (болезни), эти модели позволяют изучать начальные стадии заболевания, так как аналогичные процессы могут наблюдаться и у людей при спонтанном развитии патологии. Сюда можно отнести взаимодействие кишечной микрофлоры с клонами аутоиммунных Т-клеток и В-клеток и действие генетических факторов, регулирующих эти процессы. Очевидно, что такие модели представляют ценность при разработке и проверке эффективности диагностических и лечебных стратегий.
Методы В-клеточной терапии
Эффективные методы лечения аутоиммунных болезней, связанных с функциями В-клеток, предполагают либо прямое воздействие на патогенные В-клетки, либо воздействие на их эффекторные молекулы – то есть, на антитела. На данный момент испытаны оба подхода. Хотя к настоящему времени не было обнаружено РС-специфических антител, имеются непрямые доказательства того, что в патогенезе этого заболевания ведущая роль принадлежит гуморальным механизмам. Так, например, у части пациентов с РС имеются очаги демиелинизации с активированным комплементом, что указывает на связующее и разрушающее действие антимиелиновых аутоантител, это явление обычно обозначают термином «развитие очага демиелинизации по типу II» (см. выше). Об этом свидетельствуют результаты небольшого исследования с участием пациентов у которых наличие очагов демиелинизации типа II было подтверждено с помощью биопсии мозга. Лечение с помощью плазмафереза, который удалял из плазмы антитела, включая аутоантитела из общего круга кровообращения, заметно облегчал протекание фульминантной атаки.
В-клеточная терапия вполне может применяться и в других случаях. Наиболее успешный метод анти-В-клеточной терапии подразумевает применение моноклональных антител против В-клеток CD20. Экспрессия CD20 характерна для многих типов В-клеток – от пре-В-клеток до популяций зрелых В-клеток, однако в плазмоцитах такая экспрессия отсутствует.
В ходе исследования, которое стало научным прорывом, инфузия ритуксимаба, являющегося химерическим моноклональным антителом, приводила к значительному уменьшению очагов поражения в ЦНС. Эффективность терапии моноклональными антителами против CD-20 была подтверждена в ходе многих последующих исследований. Авторы этих исследований к тому же обнаружили относительно низкий уровень заболеваемости прогрессивной мультифокальной лейкоэнцефалопатией – оппортунистической инфекцией вирусной природы, которая неоднократно обнаруживалась в ходе других исследований, посвященных иммуномодулирующим терапиям. Механизм терапевтического воздействия ритуксимаба не нашел должного отражения в научной литературе. Тем не менее, к настоящему времени понятно, что это моноклональное антитело воздействует в первую очередь на В-клетки – но не на плазмоциты. Оно нарушает те функции В-клеток, которые не связаны с антителами как, например, презентация антигена или выработка цитокина (Врезка 1).
Третий тип подхода к лечению РС, связанный с ограничением активности В-клеток, точнее, с нейтрализацией факторов роста В-клеток, оказался менее удовлетворительным. Нейтрализация факторов роста, принадлежащих к семейству TNF (BAFF), которые имеют огромное значение для выживаемости В-клетки, не только не оказалось эффективной для лечения РС, но парадоксальным образом вызывала ее обострения. Эта неудача стала неприятным сюрпризом, принимая во внимание тот выраженный положительный эффект, который обеспечивает нейтрализация BAFF/TACI при других В-клеточных аутоиммунных заболеваниях – например, при системной красной волчанке.